Rafael Cardoso Teixeira
Em um dado momento no espaço, a partir de um núcleo extremamente condensado, há cerca de aproximadamente 13,7 bilhões de anos antes do presente, houve o momento da “Grande Explosão”, quando foram criados o espaço (Figura 1) e o tempo, concomitantemente com a gigante liberação de energia em um nível incrível, estimado em aproximadamente de 3 bilhões de graus centígrados.
Este momento primordial é denominado de “Big Bang” (termo universal), ao qual marca o surgimento do universo, e este continua a sua expansão e consequentemente a se esfriar, pois de maneira análoga a um balão de gás (Figura 1), conquanto as leis de conservação da física forçam a queda da temperatura conforme se aumenta o volume do recipiente (constante de pressão).
A partir deste momento, com tempo de
0,01s de existência, com o espaço recém criado (Primevo), este se preencheu de
radiação e de partículas fundamentais, denominadas de “quarks” (além de múons,
táons, neutrinos e suas respectivas antipartículas) que se entrechocavam à todo
momento em alta constância, produzindo e se aniquilando, devido à extrema
temperatura (3 bilhões de graus centígrados), onde tudo era energia e luz.
Essa grande quantidade de energia vem
se tornando cada vez menor à medida que o universo se expande, sendo
concomitante à expansão do universo e o consequente esfriamento. Assim, é
estimado que em cerca de 3 minutos após o momento primordial, a temperatura
diminuiu para aproximadamente 1 bilhão de graus centígrados, temperatura a qual
era baixa o suficiente para permitir a união dos quarks e a formação de
partículas com maior organização, os prótons, elétrons e nêutrons,
possibilitando a formação de partículas mais evoluídas, átomos e moléculas.
Onde se dá início ao processo de nucleossíntese primordial.
Com o nascimento dos átomos e das
moléculas, passa a ocorrer uma mudança de extrema importância, onde o universo começa
a deixar de ser dominado exclusivamente por partículas energéticas,
estritamente radiação. A partir da formação dessas partículas a matéria começa a dominar a sequência de
eventos. Uma das principais consequências, à priori, é o surgimento da
gravidade, em nível de escala local, não de universo, provocando a condensação
de matéria.
O que é importante destacar, de
início, antes da sequência de formação dos elementos químicos descobertos nos
diversos sistemas físicos do Universo, é que estes foram formados basicamente
por três grandes tipos ou classes de processos, em sequência: nucleossíntese primordial, nucleossíntese estelar e nucleossíntese interestelar.
É relevante destacar também que o
Universo é possivelmente composto de diversas espécies de elementos: matéria
escura (70% - não se sabe o que é), matéria escura fria (25% - não se sabe o
que é), Hidrogênio e Hélio gasosos (4%),
Hidrogênio e Hélio em estrelas (0,5%), neutrinos (0,3%) e elementos
pesados (0,03%). Onde os elementos pesados (0,03%) são o que os astrônomos
chamam de tudo que não é H e He, ou seja, toda a tabela periódica com a exceção
destes dois elementos.
O primeiro elemento ou núcleo a se
formar nesta sequência de condições (temperatura, pressão e disponibilidade de quarks
e partículas) foi o Deutério[1]
(Esquema 1), que é o isótopo do Hidrogênio (H), ao qual contém somente 1 próton
e 1 nêutron. Com a consequente diminuição progressiva da temperatura, resultando
na finalização dos mecanismos termonucleares, ocorre o que Hubert Reeves
(astrofísico nuclear) denominou de “primeira
crise de crescimento da complexidade”.
Essa primeira crise considerada perdura
por volta de 1 milhão de anos, tendo situação satisfatória para o início do
comando da energia eletromagnética, possibilitando portanto à formação do
primeiro elemento químico: o Hidrogênio (H).
Já a formação do Hélio (He – Figura 2) se forma quando a temperatura caí para 1
bilhão de graus centígrados, contendo em si 4 nêutrons e 3 prótons.
Figura 2: A formação do Hélio durante a nucleossíntese primordial. Sendo o He-4 muito estável. Fonte: http://www.astro.iag.usp.br/~ronaldo/intrcosm/Glossario
Este estágio inicial (Nucleossíntese Primordial) da expansão e resfriamento do universo é de altíssima intensidade, sendo denominado de “Nucleossíntese Primordial”. Nesse estágio, é que dá razão à abundância de H e He no universo, como apontou primeiramente o cientista russo-norte-americano George Gamow (1904-1968), afirmando que o H e He correspondem, respectivamente, a 74% e 24% de toda a massa do Universo (Tabela 1).
 Tabela
1: abundância relativa de elementos
químicos no Universo, o Sol e a Terra, os % são aproximados. Fonte: Introdução:
a distribuição dos elementos químicos. Fonte: MACIEL, W. J (2004).
Tabela
1: abundância relativa de elementos
químicos no Universo, o Sol e a Terra, os % são aproximados. Fonte: Introdução:
a distribuição dos elementos químicos. Fonte: MACIEL, W. J (2004).Esta Tabela 1 demonstra que a
quantidade e distribuição dos elementos químicos é complexa. Onde a massa do
universo é constituída basicamente de H e He, e os demais 2% é o total de
elementos mais pesados, ou seja, com Z > 2 (número atômico > 2). O que
comparado à Terra é como “uma acaso da natureza”, pois a maior parte material
do nosso planeta e dos seres vivos, incluindo nós seres humanos, é composto por
parte dessa pequena porcentagem e elementos com Z > 2.
Em sequência (Esquema 1) se encontra,
de forma simples, a formação ou fusão do H a partir de prótons, passando pelo
deutério até se formar o He, chamado de ciclo próton-próton (ciclo p-p), de
acordo com a vídeo-palestra de COSTA (2018):
Esquema 1:
sequência de formação do Deutério (D) ao Hélio (He) – ciclo p-p.
- dois 3He colidem formando um 4He
mais dois prótons disponíveis para o ciclo seguinte.
Para este processo é importante
compreender a relação de energia, tendo a seguinte pergunta em mente: qual é o
balanço energético desta reação? A resposta se encontra na sequência.
. He4: 4.002603
Observe que existe uma diferença de 0.028805
(ou 0,7% da massa), onde essa diferença representa o que se converteu em energia liberada pelo processo.
Nucleossíntese
Primordial
Está fase se inicia em um momento
extremamente rápido, em torno de 3 minutos após o momento inicial, o Big Bang.
Nesta primeira fase se dá a formação desde o H até o Berílio (Be). Quando a temperatura baixou para valor
aproximado de 2.727 °C
(3000 kelvin), a nucleossíntese primordial cessou devido a não existir mais
calor em quantidade necessária para o prosseguimento das reações de formação de
novos elementos químicos além, estagnando-se no H e He, estando o Universo em
fase de desacoplamento da matéria e da radiação (Figura 3).
Figura
3 - Desacoplamento da matéria e radiação. Fonte: INPE. Disponível em: http://t1.gstatic.com/images.
Nessa fase da nucleossíntese primordial além da formação do D (2H),
tem-se a formação do trítio (3H), e isótopos 3He, 4He
e 7Li. Onde o processo de formação desde o D até o Lítio (Li) é
esquematizado a seguir:
Neste momento é clara a determinação
da abundância dos elementos Deutério, He e Li, os quais são uma marca, um
termômetro dessa primeira etapa dos processos de nucleossíntese, onde a queda
da temperatura possibilitou a montagem dos núcleos citados acima a partir dos
prótons e nêutrons livres.
O processo se faz pela relação das
unidades existentes neste momento primordial, onde se estima que havia 1
nêutron para cada 7 prótons. Rapidamente havia a combinação de 1 nêutron e 1
próton, e depois a totalidade deles se combinaram para formar o He. Sobrando
assim, 6 prótons sem emparelhamento.
O processo de formação desde o H até
o Li se dá por reações de fusão nuclear, onde desde o Esquema 1, a sequência
gerou elementos mais estáveis, o Li e o Be. Onde o 7Be é a combinação
de 3He mais 4He, já o 7Li é a combinação do 7Be
mais um elétron. Por causa do curto espaço de tempo em que a nucleossíntese
primordial ocorreu, parando pela expansão do universo, nenhum elemento
mais pesado do que o Be poderia ser formado. Talvez, o B. É destacado que as
reações de fusão cessaram até o Li, causado por duas principais razões de
acordo com Costa e Hovarth (2016): i) inexistência de núcleos estáveis entre 5
e 8 núcleos, e ii) expansão que diluiu a densidade e impediu que a fusão
continuasse. Até este momento estimasse que havia se passado 20 minutos pós o
momento inicial.
Lembrando da questão do início do
fenômeno de gravidade, a partir da nucleossíntese primordial, tem-se a
sequência de a matéria primordial acomodar-se em pequenas irregularidades
(potencial gravitacional local). Essa matéria aglomerada passou a crescer,
aumentando assim seu potencial gravitacional, onde a maior concentração de
matéria aglomerada gerava como consequência a formação das grandes estruturas:
estrelas e galáxias. Sendo que a partir deste momento é que as estrelas, sendo
os “fornos nucleares”, que vão permitir a continuação da nucleossíntese até a formação
completa da tabela periódica.
Nucleossíntese
Estelar
A formação das massas estelares se
inicia pela condensação de matéria a partir da gravidade local (que tende a
aumentar à medida que os corpos aumentam de tamanho). Assim, as estrelas
formadas e em formação são classificadas de acordo com a sua massa. A massa em
comparação é relativa à do Sol (2 x 1030 kg), portanto as massas das
estrelas são ordenadas pela massa solar (MSol) e são classificadas em:
i) estrela de baixa massa – entre 0,08 e 0,8 MSol;
ii) estrela de massa intermediária – 0,8 a
8 MSol;
ii) estrela massiva – maior que 8 MSol.
As estrelas que
possuem massa menor que 0,08 MSol não possuem capacidade de realizar o processo
de fusão nuclear do H, e portanto, não são capazes de contribuir para a formação
dos demais elementos químicos que conhecemos e se encontram catalogados na
tabela periódica.
As estrelas agem a
partir de reações termonucleares, onde os H são fundidos em He e estes são
fundidos em núcleos mais pesados, processo que contêm cada vez maior intensidade
e valor de temperatura. Já para a formação do C, de extrema importância, ao
qual é produzido pelo processo triplo-alfa em todas as estrelas, devido a sua
formação ser proveniente de He, sendo o pontapé de todo o processo de
nucleossíntese.
Outro ciclo de
importância nas formações de elementos químicos nas estrelas é o chamado ciclo
CNO (Carbono-Nitrogênio-Oxigênio). Em que nas estrelas mais massivas o NCO é o processo dominante, sendo catalítico
e utiliza os três elementos (CNO) como intermediários na formação de um núcleo
de He. Veja a seguir o esquema:
O processo acima é simples e inicia com um próton (p - 1H) que choca com um núcleo de C (12C) dando origem a um isótopo radioativo de N (13N). Tem-se como resultado a liberação de radiação-gama (γ). O núcleo de N libera pósitron mais neutrino, modificando-se para um isótopo de C (13C). Com o choque de mais um próton com este núcleo de C, dá-se a conversão para um isótopo estável de N (14N) mais a liberação de radiação-gama.
Ao ser atingido por mais um próton, o núcleo de N é
então convertido em um isótopo de O (15O), liberando mais raios
gama. O elemento O decai para o isótopo de N (15N) liberando
neutrino mais pósitron. Finalmente, o choque de outro próton quebra o 15N
em um núcleo de H (4He) e o átomo de C inicial (12C), possibilitando
a continuidade do ciclo. Observe que toda energia é liberada na forma de raios
gama e neutrinos (partículas neutras leves que escapam para o espaço na
velocidade da luz), enquanto os pósitrons que são formados acabam sendo destruídos
por seu correspondente em antimatéria, os elétrons.
Observe que a sequência dessas
reações usa núcleos de C preexistentes, produzindo temporariamente N e O,
concluindo ao final a restituição do C inicial. Tendo também os produtos como
He mais pósitrons (e+), neutrinos (ve) e energia.
A evolução prosseguirá principalmente
se a estrela possuir MSol suficiente para provocar a ignição do He e se
transformará em C pelo processo chamado de “triplo-alfa”:
A partir destes dois ciclos (p+p e CNO) abre-se o caminho para a
compreensão de ciclos nucleares mais complexos e superiores que dão origem à
parte dos elementos da tabela periódica e a análise e compreensão dos processos
de explosões nucleares. Onde os processos de nucleossíntese são realizados
apenas no seu núcleo e não em todo o seu corpo. Dessa forma, os elementos
químicos produzidos ficam aprisionados até a conclusão do ciclo evolutivo da
estrela, sendo liberado e gerando enriquecimento no meio interestelar e de
futuras estrelas (planetas e corpos celestes variados) e por meios de vários
possíveis mecanismos de ejeção. Que geram as “nebulosas planetárias”, que são
ricas em elementos químicos provenientes de suas estrelas de origem.
O material produzido nos núcleos
estelares são ejetados por meio de explosões, que podem ser divididas em dois
tipos básicos no meio interestelar: as novas
e as supernovas. As novas são explosões de estrelas
pertencentes aos sistemas binários (sistema estelar que consiste de duas
estrelas orbitando um baricentro - centro de massas – em comum). Enquanto as supernovas são resultantes de colapsos
de estrelas massivas, onde a estrela se desmancha por completo no ato da
explosão.
O processo de formação dos elementos
químicos apresentados até agora descreveram a formação do H, do He, do Li e do C.
Não falamos sobre a formação do Boro (B), pois este se forma de maneira
especial, a chamada “espalação”, que ocorre pelo processo de nucleossíntese interestelar, consistindo
neste caso na colisão de raios cósmicos contra núcleos atômicos. Onde a
“espalação” é responsável pela produção de praticamente todo o Li, Be e B
existentes no Universo, portanto é um processo fundamental, sendo que apenas
uma pequena fração do total de Li e Be foi produzido no Big Bang.
O geólogo Claude Allègre calcula que
“apenas 10% das estrelas desempenham um papel fundamental” na variedade dos
elementos químicos. Onde apenas 1% das estrelas fabricam elementos pesados e
90% das estrelas limitam-se a queimar H e fabricar He.
Supernovas e a formação do elementos pesados
As estrelas massivas, cuja massa é de no mínimo 8 vezes a do Sol (esse valor é aproximado, pois depende também da composição química da estrela), conclui a sua existência com a explosão e consequente formação de uma supernova. Um evento que é de grande proporção, sendo uma catástrofe. Porém, proporciona a formação de todos os elementos massivos da sequência de massas atômicas pós Ferro (Fe), como demonstrada na tabela periódica (Figura 4). Outra informação importante a ser destacada é que as estrelas massivas possuem ciclos evolutivos muito rápidos.
Essa velocidade do ciclo tem relação
direta com o tamanho da MSol, pois à medida que a massa aumenta, sua
luminosidade também é maior, o que esgota mais rapidamente o combustível nuclear e, portanto, diminui o
tempo de seu ciclo evolutivo.
Diversos estudos compreenderam que as
estrelas com 8 a 10 vezes a MSol não chegam a ter temperaturas que permitem a
sequência de ciclos mais avançados, resultando em um caroço constituído de
Oxigênio (O), Neônio (Ne) e Magnésio (Mg), onde ao ultrapassar o seu limite de
pressão o caroço implode e expele os elementos. Para os elementos mais pesados
que o Fe, que se encontram na estrela, ao ultrapassar o Limite de Chandrasekhar
(equivalente a 1,44 MSol) o núcleo da estrela colapsa quase em queda livre.
Após isso, forma-se uma estrutura com 10 a 15 km de diâmetro composta de
nêutrons e um caroço agora de Fe e não mais de O-Ne-Mg. A temperatura deste
colapso pode chegar a 100 bilhões de Kelvin.
Outra forma de uma estrela evoluir
até explodir como supernova é a dos
sistemas binários, composto por estrelas extremamente massivas uma próximo da
outra, sendo uma delas a anã branca. À
medida que uma evolui, pode haver troca de massa até que a anã branca ultrapasse o Limite de Chandrasekhar. Como a anã branca possui uma quantidade
relativa de C, este pode ser fusionado para elementos de massa próximos ao Fe.
Com a formação dos núcleos de Fe,
ocorrem mudanças na nucleossíntese dos elementos mais leves. A fusão nuclear
não é mais exotérmica depois dessas massas atômicas, onde a formação de
elementos mais pesados passa a ocorrer especificamente pela captura de
nêutrons. Onde essas formações são divididas em dois grupos de captura: processos
s (slow – lento) e processos r (rapid – rápido).
O processo s se faz em
ambientes que possuam nêutrons livres, mas com densidade baixa, onde um núcleo
só poderá capturar um nêutron e emitir um elétron, sendo chamado de decaimento
beta nuclear. Esse processo desenvolve a formação de elementos químicos em uma
sequência que vai do 57Fe até o 209Bi, como é mostrado
uma parte dessas reações no esquema abaixo.
O processo s tem capacidade
de formar até o 209Bi, a nucleossíntese dos elementos mais massivos
necessitam de uma fonte mais abundante de nêutrons. Essa alta densidade de
nêutrons ocorre durante a explosão de uma supernova,
constituindo-se no processo de captura rápida de nêutrons (processo r).
A maior densidade de nêutrons costuma
ocorrer durante os primeiros 15 minutos após o colapso de um estrela massiva e
a explosão de uma supernova,
configurando uma alta densidade de nêutrons e consequentemente a formação de
núcleos estáveis mais pesados. Esse processo também é chamado de “nucleossíntese explosiva”.
A partir desta nucleossíntese ocorre
a produção de elementos mais pesados, onde dá origem a fusão de elementos leves
em elementos com maior peso, criando elementos como Si, S, Cl, Ar, K, Ca, Sc,
Ti, V, Cr, Mn, Fe, Co e Ni. Sendo estes denominados de elementos primários,
pois podem ser fundidos a partir de H e He puro em estrelas massivas. Enquanto
elementos mais pesados que o Ni são formados pelo processo r.
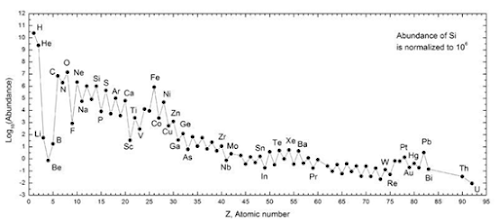
Observe no Gráfico 1 que estes
elementos citados anteriormente são muito mais abundantes no espaço, comparando-os
aos elementos mais pesados que o Ni.
A estrela chamada de supernova pode ocorrer em dois tipos de
cenários:
I) quando uma estrela anã branca passa por uma explosão nuclear e atinge o seu limite de
Chandrasekhar[2]
e depois absorve a massa de uma estrela vizinha, que normalmente é uma gigante
vermelha.
II) se trata de um evento mais comum, sendo causado
por uma estrela maciça, normalmente uma supergigante, atingindo o 56Ni
relacionado aos processos de fusão nuclear, onde este isótopo tem decaimento
radioativo em 56Fe produzindo uma liberação de energia por fusão
nuclear exotérmica. Este processo resulta na fusão do material, por altas
pressões e densidades, liberando energia e criando uma zona de dispersão do
material da estrela para o meio interestelar.
Outras dinâmicas de processos são
responsáveis pela nucleossíntese de elementos mais pesados, processos que são conhecidos
como processo
rp-e, ao qual capturam prótons por meio de fotodesintegração[3]
envolvendo o processo-gama (ou processo-p).
Após a estrela finalizar o seu
processo de queima de O, seu núcleo se torna composto de Si e S, onde há
temperatura suficientemente alta, o Si e demais elementos são fotodesintegrados
por energia. A queima do Si é diferente dos estágios anteriormente citados na
nucleossíntese, criando uma sequência específica, contrastada por reações
inversas tendo captações de partículas-alfa e ejeção. A sequência é:
28Si + 4He ↔ 32S +
fóton;
32S + 4He ↔ 36Ar +
fóton;
36Ar + 4He
↔ 40Ca + fóton;
40Ca + 4He
↔ 44Ti + fóton;
44Ti + 4He
↔ 48Cr + fóton;
48Cr + 4He
↔ 52Fe + fóton;
52Fe + 4He ↔ 56Ni +
fóton;
e
por fim 56Ni + 4He ↔ 60Zn + fóton
A queima explosiva da supernova provoca um choque, passando
pela queima de Si, onde este é o principal elemento contribuinte para a
nucleossíntese dos elementos do intervalo de massa entre 28 e 60,
correspondentes do Ni ao Nd. Isso ocorre porque a estrela não pode mais liberar
energia através da fusão nuclear devido um núcleo com 56 núcleons e por possuir
menor massa por núcleon. O passo seguinte na cadeia de partículas-α seria o 60Zn,
que tem um pouco mais de massa por núcleo e, portanto, é menos
termodinamicamente favorável. Mas pela meia-vida do 56Ni ser bastante
rápida, em poucos minutos este decaí dentro do núcleo de uma estrela maciça.
Portanto, a formação dos elementos químicos presentes hoje no universo demandou uma complexa relação entre tempo, energia (temperatura), disponibilidade de partículas fundamentas e processos químicos fundamentais e/ou complexos, além da somatória dos processos de nucleossíntese: a primordial, a estelar, a explosiva e a interestelar.
Assim, a base química de toda a terra, os componentes dos constituintes inorgânicos (atmosfera, hidrosfera, litosfera e pedosfera) e orgânicos como a biosfera e noosfera (esfera social) são provenientes de todo este prolongado e complexo processo de formação dos elementos químicos.
[1] Os isótopos são átomos cujos núcleos têm o mesmo número de prótons, mas números diferentes de nêutrons. Nem todos os átomos do mesmo elemento são idênticos e cada uma dessas variedades corresponde a um isótopo diferente. Cada isótopo do mesmo elemento tem o mesmo número atômico (Z), mas cada um tem um número de massa diferente (A).
[2] quando a massa do núcleo superar um determinado limite.
[3] Fotodesintegração é um processo no qual raios gama de energia extremamente alta interagem com um núcleo atômico e causam uma extrema excitação deste, o qual imediatamente decai em dois ou mais núcleos filhos.
Referências
Bibliográficas
ALLÈGRE, C. 1999. Introdução à Uma História Natural.
Ed. Teorema, Lisboa, pp. 259.
ANDERS, E. & GREVESSE, N. 1989. Abundances of the elements: Meteoritic and solar. Geochimica
et Cosmochimica Acta. Vol. 53. pp. 197-2014.
BARRETO, F. C. S.; VAZ, P. R.; FRANCO, G. A. P. 2012.
O Universo Vivo. Rev. UFMG, Belo Horizonte, v.19, n.1 e 2, pp.182-205.
COSTA,
R. D. D. & HOVARTH, J. E. 2016. A Origem dos Elementos. In: Astrobiologia
[livro eletrônico]: uma ciência emergente / Núcleo de Pesquisa em
Astrobiologia. - São Paulo: Tikinet Edição: IAG/USP, pp. 390.
COSTA,
R. D. D. 2018. A origem dos elementos químicos. Disponível em: https://youtu.be/snnAWiRHCd4.
Acesso em: 11 out. 2018.
MACIEL, W. J. 2004. Formação dos elementos químicos .
Revista USP, n. 62, pp. 66-73.
PEDROSA, L. A. 2013. DO BIG-BANG AO URÂNIO: As
Nucleossínteses Primordial, Estelar e Explosiva - Uma abordagem para o Ensino
Médio. Belo Horizonte, MG, Pontifícia Universidade Católica de Minas Gerais.
168p. (Dissertação de Mestrado).
TERUYA, N. & DUARTE, S. B. 2012. Núcleos Exóticos
e Síntese do Elementos Químicos. Quim. Nova, Vol. 35, No. 2, pp. 360-366.







Nenhum comentário:
Postar um comentário